
Batterien
Langjährige Erfahrung und biobasierte Anwendungen ermöglichten es Jongia, in das neue und schnell wachsende Geschäftsfeld des Energiemarktes vorzustoßen. Die Rühr- und Mischanlagen von Jongia erfüllen extreme Kriterien hinsichtlich Emissionswerten, Wellenausrichtungstoleranzen und Rotationsgenauigkeit.
Batterie Chemikalien mit Jongia Mixing Technology!
Batteriechemikalien können in drei Hauptkategorien eingeteilt werden,- Elektrolyte für sekundäre Lithium-Ionen-Batterien,
- Elektrolyte für Lithium-Primärbatterien,
- Elektrolyte für Superkondensatoren.
Die neuesten Energiemärkte erfordern Mischtechnik mit geringstem Stromverbrauch

Elektrolyt für eine Million Elektroautos
Anwendungen
Batterien erklärt
Die Chemie einer Batterie

Häufig gestellte Fragen
Welches sind die wichtigsten Kategorien von Batteriechemikalien?
Batteriechemikalien können in drei Hauptkategorien eingeteilt werden: Elektrolyte für sekundäre Lithium-Ionen-Batterien, Elektrolyte für primäre Lithium-Batterien und Elektrolyte für Superkondensatoren. Jede Kategorie spielt eine entscheidende Rolle für die Leistung und Effizienz der verschiedenen Batterietypen.
Wozu dient der Elektrolyt in Lithium-Ionen-Batterien?
Der Elektrolyt in Lithium-Ionen-Batterien, der aus einem Lösungsmittel und einem Lithiumsalz besteht, ist für den Transport der Lithium-Ionen von entscheidender Bedeutung. Er ist das „Blut“ der Batterie und sorgt für eine hohe Spannung und spezifische Energie, was zur Gesamtleistung und den Vorteilen der Batterie beiträgt.
Welche Rolle spielt Jongia bei der Batterieproduktion?
Jongia liefert maßgeschneiderte Rührwerke für den Elektrolytproduktionsprozess in einer neuen Fabrik in Polen. Unsere Ausrüstung ist auf die besonderen Anforderungen der Elektrolytproduktion zugeschnitten und stärkt Jongias Ruf als wichtiger Akteur auf dem Markt der Batterieproduktion.
Was sind die Bestandteile einer Batterie?
Eine Batterie besteht normalerweise aus drei Teilen: der positiven Elektrode (Anode), der negativen Elektrode (Kathode) und der Elektrolytlösung. Diese Komponenten arbeiten zusammen, um den Stromfluss zu erleichtern, wenn sie an ein Gerät angeschlossen sind.
Wie werden sich die Lithium-Ionen-Batterien in Zukunft entwickeln?
Es wird prognostiziert, dass Lithium-Ionen-Batterien die Energiespeicherlösungen dominieren werden, wobei die weltweite Produktion erheblich steigen wird. Fortschritte in der Technologie und die wachsende Nachfrage nach Elektrofahrzeugen und erneuerbaren Energien werden dieses Wachstum vorantreiben und die Batterien effizienter und kostengünstiger machen.
Energie – Kontakte

Tom Pruymboom
Verkaufsleiter
Gebiet weltweit

Jan Siert Tjeerdsma
Projektleiter
Technischer Spezialist
Energie – Verwandte Artikel

Ist die Natrium-Ionen-Batterie die nächste Generation nachhaltiger Batterien?
Die Natrium-Ionen-Batterie (NIB oder SIB) ist ein wiederaufladbarer Batterietyp, der Natriumionen (Na+) als Ladungsträger verwendet. Das Funktionsprinzip und der Zellaufbau sind fast identisch mit denen der Lithium-Ionen-Batterien (LIB), allerdings wird Lithium durch Natrium ersetzt.

Wie sieht das Recyclingverfahren für Lithium aus?
Derzeitige kommerzielle Lithium-Ionen-Batterien enthalten hauptsächlich Übergangsmetalloxide oder -phosphate, Aluminium, Kupfer, Graphit, organische Elektrolyte, die schädliche Lithiumsalze enthalten, und andere Chemikalien. Daher wird dem Recycling und der Wiederverwendung von verbrauchten Lithium-Ionen-Batterien von vielen Forschern immer mehr Aufmerksamkeit geschenkt. Aufgrund der hohen
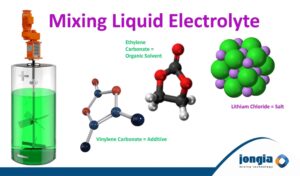
Mischen von Elektrolyt für Ionen-Lithium-Batterien
Der Elektrolyt als Grundlage für Ionen-Lithium-Batterien spielt eine Schlüsselrolle für den Transport der positiven Lithiumionen zwischen Kathode und Anode und folglich für die Lade- und Entladeleistung der Batterie. Daher muss es auf mögliche Verunreinigungen überprüft werden. Gleichzeitig ist der Elektrolyt








